ICH 于 7 月 27 日正式發(fā)布了廣受期待的 Q13 《原料藥與制劑的連續(xù)制造》指南,公開(kāi)征詢意見(jiàn)。指南“描述了連續(xù)制造(CM)的開(kāi)發(fā)、實(shí)施、操作和生命周期管理的科學(xué)和監(jiān)管考慮因素。”指南還“澄清了 CM 的概念,描述了科學(xué)方法,并提出了針對(duì)原料藥和制劑連續(xù)制造的監(jiān)管考量。”
指南適用于化學(xué)實(shí)體和治療性蛋白質(zhì)原料藥和制劑的連續(xù)制造。適用于新產(chǎn)品(例如,新藥、仿制藥和生物類似藥)的連續(xù)制造以及現(xiàn)有產(chǎn)品從批制造轉(zhuǎn)變?yōu)檫B續(xù)制造。另外,指南指出,指南中的原則也可能適用于其它生物/生物技術(shù)實(shí)體。
新發(fā)布的指南草案現(xiàn)已進(jìn)入 ICH 流程的第 2 階段,在此階段,ICH 大會(huì)將向地區(qū)監(jiān)管機(jī)構(gòu)發(fā)布共識(shí)草案,以供內(nèi)部咨詢和公眾評(píng)議。ICH Q13 由一個(gè)主體指南和五個(gè)附錄組成;指南討論了不同的連續(xù)制造模式,并審查了控制策略和監(jiān)管考慮。
指南草案中描述了三種不同的連續(xù)制造模式:
制造方法的組合,其中一些單元操作以批處理模式運(yùn)行,而其它單元操作則集成并以連續(xù)模式運(yùn)行;
原料藥或制劑生產(chǎn)過(guò)程的所有單元操作被集成并以連續(xù)模式運(yùn)行;
原料藥和制劑單元操作跨越原料藥和制劑之間的邊界集成形成單一連續(xù)制造過(guò)程(即,原料藥通過(guò)集成單元操作連續(xù)形成和加工以生成最終藥品制劑)。
指南中指出,在這三種連續(xù)制造模式下的任何一種制造方法都可以結(jié)合緩沖管線或儲(chǔ)罐,保持物料輸入和輸出的恒定流量。
指南的正文部分介紹了通常不特定于技術(shù)、劑型或分子類型的連續(xù)制造的基本方面。指南的五個(gè)附錄討論了原料藥、制劑、治療性蛋白原液以及原料藥和制劑集成的連續(xù)制造,并包含了一個(gè)有關(guān)管理干擾的觀點(diǎn)的附錄,通過(guò)提供特定于某些模式、技術(shù)和生產(chǎn)方法的說(shuō)明性示例和考量因素,用以補(bǔ)充指南正文。
指南將 ICH Q7 的批次定義合并到連續(xù)制造中。一批被定義為由輸出物料的量、輸入物料的量或在定義的定義的質(zhì)量流量下的運(yùn)行時(shí)間組成。根據(jù)指南,其它“科學(xué)合理”的方法也被考慮用于定義批次。
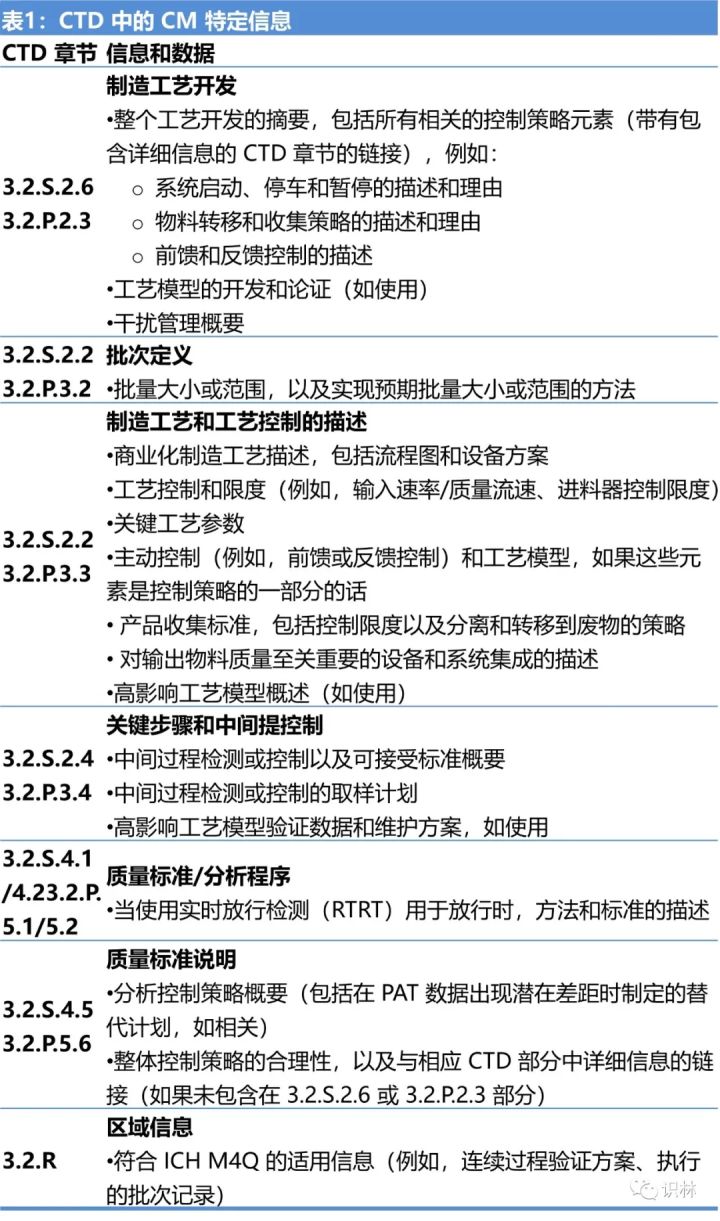
指南中還用專門(mén)的一節(jié)介紹了在通用技術(shù)文件(CTD)中如何提交關(guān)于連續(xù)制造的特定信息,見(jiàn)下表。在原料藥和制劑集成連續(xù)制造的情況下 , 一些信息和數(shù)據(jù),例如集成流程圖可能會(huì)在 CTD 3.2.P 中提供,并在 3.2.S 中交叉引用。
ICH 專家工作組計(jì)劃于 2021 年 11 月舉行面對(duì)面會(huì)議 , 討論收到的反饋意見(jiàn),并計(jì)劃于 2022 年 11 月簽署文件 , 將指南推進(jìn)到第 3 階段,隨后采納實(shí)施指南。
作者:識(shí)林-藍(lán)杉
來(lái)源:識(shí)林